(文章轉載自EurekAlert!,原刊於2024年1月4日)
香港科技大學(科大)領導的研究團隊成功研發出一種光學等離子體鑷子控制的表面增強拉曼光譜(SERS)平台,利用光的開關控制,以單分子水平探測混合物中不同的胰島類澱粉蛋白質物種,揭示pH影響下胰島類澱粉蛋白的異質結構,以及與第2型糖尿病相關的澱粉樣聚集機制背後的秘密。
單分子技術能夠分辨每個分子的訊息,透過去除整體取平均的模式獲得被傳統宏觀表徵方法掩蓋的細節,革新我們對複雜性和異質性較高體系的認知。目前,單分子的實驗條件通常要依靠高度稀釋和/或分子固定的方法來實現,因為受到光學衍射極限的限制,探測體積難以進一步減少。然而,某些生物分子體系參與的各種相互作用在很大程度上受到濃度的影響。例如,人類胰島澱粉樣多肽(Amylin,hIAPP)是一種天然無序蛋白,缺乏穩定的二級結構,但是會受到濃度、酸鹼度等環境因素調控從而產生聚集的傾向,在2型糖尿病患者中形成各種各樣的寡聚體中間體和澱粉樣纖維。這些分子機制仍然未明,因為目前很難從動態轉變的混合物中檢測到稀有、瞬態和形式各異的澱粉樣多肽物種,所以需要開發更先進的單分子研究方法。
最近,由科大化學系助理教授黃晉卿教授領導的研究團隊取得了重大突破,成功開發了一種新穎的單分子平台,結合光學等離子操控和SERS測量技術,可以減少以往受到光學衍射限制的檢測體積,並增強分子訊號,從而能夠在生理濃度下高通量地表徵受酸鹼度影響的澱粉樣多肽物種。
具體來說,團隊建構出在兩個塗有銀奈米顆粒的二氧化矽微珠之間的等離子體結合點,在雷射照射下捕捉固定一個額外的銀奈米顆粒,形成一個動態奈米腔,可以夾住單一或少量分子進行靈敏的SERS表徵。由於光學等離子體操控和SERS現象只發生在奈米尺度的狹小空間內,因此能克服光學衍射極限,實現精確的位置控制,最小化檢測體積,並同時提升SERS增強效果。此外,在溶液中,塗有銀奈米顆粒的二氧化矽微珠二聚體比傳統的銀奈米顆粒組裝體更穩定,便於在普通顯微鏡下看到,幫助定位等離子體結合點,提高效率和可重複性。只要將雷射光源在「開」與「關」狀態之間切換,就能有效控制光學等離子體對銀奈米顆粒的操控,調控動態奈米腔的組裝和解離,實現高通量取樣與SERS的同時測量。
利用這個高效的單分子平台,研究團隊在胰島β細胞分泌顆粒的酸鹼度pH 5.5和細胞外區域的酸鹼度pH 7.4這兩種不同的生理條件下,獲得了大量具有統計意義的SERS光譜,揭示了各種澱粉樣多肽物種的結構特徵。在中性條件下,團隊鑑別出兩種罕見的澱粉樣多肽物種,並且得到了分子動力學(MD)模擬的論證。在澱粉樣聚集的早期階段,這兩種罕見物種與大量無結構的澱粉樣多肽單體共存,分別具有關鍵的轉折結構或具有短β-捲髮結構和受限的C端構型。這個不同澱粉樣多肽物種之間的微小平衡偏移,即使在將pH從7.4調整到5.5後,也能驅動不可逆的澱粉樣發展。因此,直接對這些澱粉樣多肽物種在混合中進行結構表徵,可以揭示pH對它們的分子內和分子間相互作用的影響,有助於揭示pH調控的澱粉樣聚集機制,進而為了解2型糖尿病提供啟示。
黃教授表示:「我們提出了一個簡單易行的策略,可以同時實現減少檢測體積、增強分子訊號和提高採樣週轉效率。這個單分子平台可以獲得大量的SERS光譜作為分子快照,與透過分子動力學(MD)模擬獲得的資訊相媲美。透過對單分子層面的結構細節進行統計分析,我們能夠重建整體的平均特性,並獲得異質混合物中關於特定分子類型的出現機率和存在數量的獨特洞察力,具有揭示複雜系統中隱藏奧秘的潛力。」
這項研究最近已在科學期刊《自然–通訊》上發表。
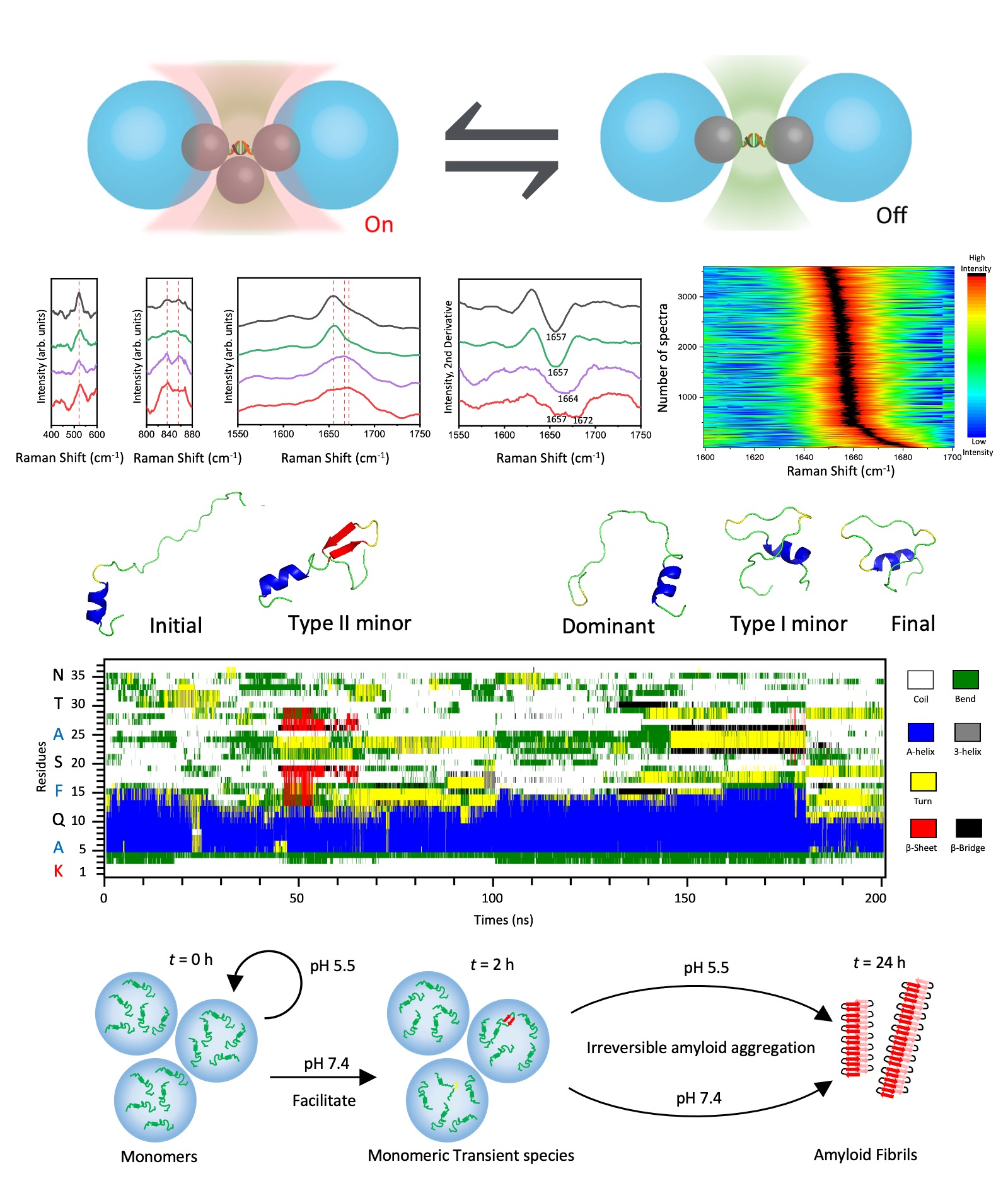
單分子平台的示意圖以及基於表面增強拉曼散射(SERS)表徵和分子動力學(MD)模擬的pH依賴性胰島類澱粉蛋白的異質結構特徵




