(文章转载自EurekAlert!,原刊于2023年12月6日)
由香港科技大学(科大)领导的研究团队,近日揭示类胰岛素生长因子2 (IGF2) 如何调控肌肉干细胞分化,这对通过抑制IGF2分泌以操控其讯号路径的潜在治疗策略提供理论基础。
IGF2在细胞增殖、迁移、分化和存活等过程中起着关键作用。 它的功能失调会导致多种生长障碍,包括银罗素综合症 (Silver–Russell syndrome) 和贝克威思–威德曼症候群 (Beckwith–Wiedemann syndrome)。 虽然IGF2的表达和其激活的下游讯号传导途径已被广泛研究,但新合成的IGF2蛋白如何高效地分泌以发挥其功能仍然未明。
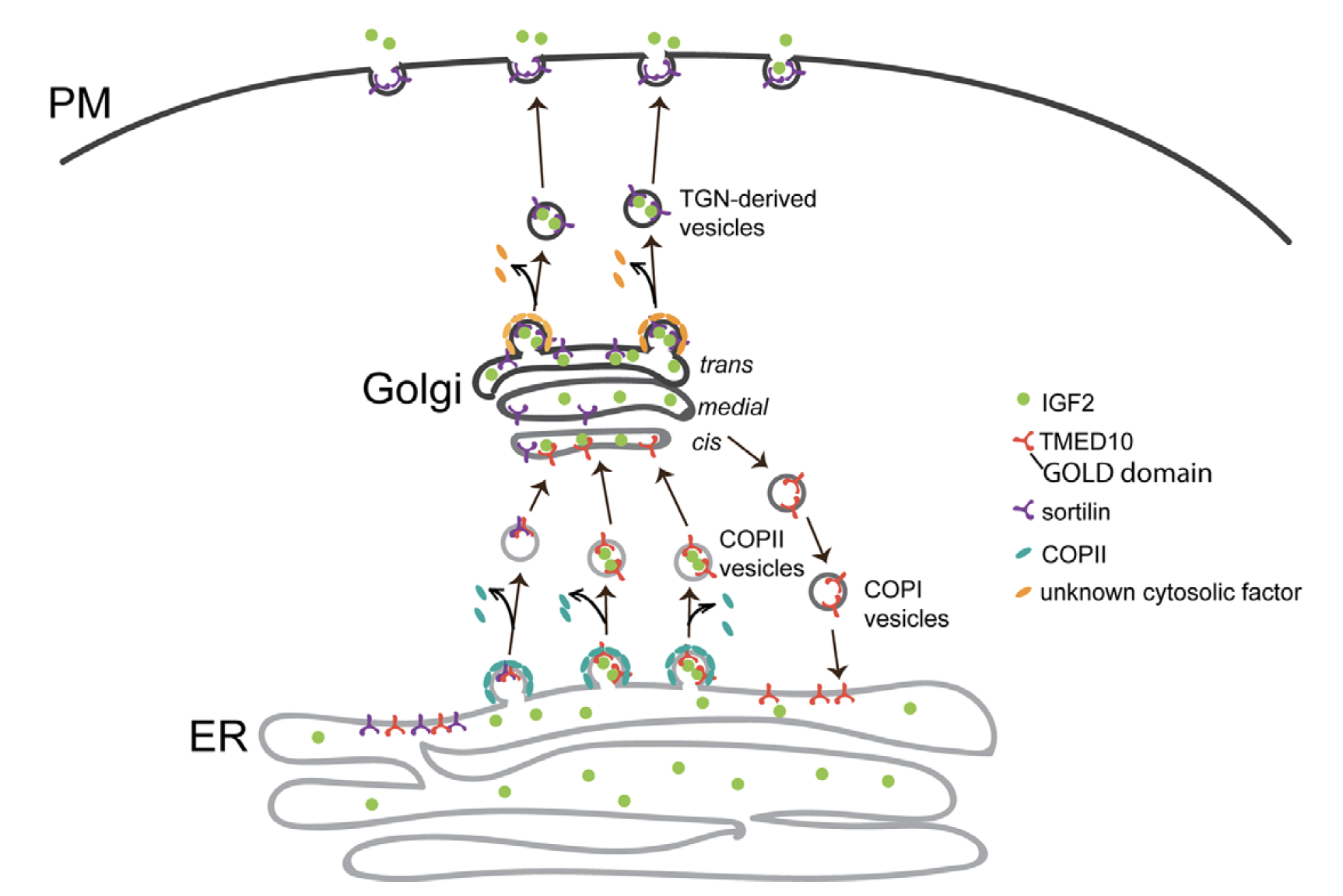
近日,由科大生命科学部副教授郭玉松所领导的团队发现,新合成的IGF2需要经过几个细胞内转运站,包括内质网和高尔基体,才能被细胞分泌出来。 团队发现一种名为TMED10的I型跨膜蛋白,能够识别IGF2上的转运信号,从而促进IGF2从内质网到高尔基体的运输。 团队进一步研究发现,这种调控是TMED10的GOLD结构域与IGF2的112-140残基直接相互作用的结果。 此外,质谱分析显示TMED10也介导了单通道跨膜蛋白sortilin的内质网输出。 后续研究表明,sortilin有助于IGF2的高尔基体后转运,这意味着TMED10间接地介导了IGF2从高尔基上的输出。 研究团队也在小鼠的C2C12肌母细胞中验证了他们的模型,证明TMED10调节了C2C12细胞中IGF2的分泌,进而调控肌肉干细胞分化。
郭教授说:「这些发现增进了我们对IGF2的生理作用、疾病机制和潜在治疗应用的理解。 在特定条件下,IGF2信号通路的过度激发会触发不受控的细胞增长,或会导致癌症。 透过调控IGF2细胞内转运过程,我们或能调节IGF2信号通路以达到临床治疗效果。 此外,由于IGF2在组织修复和再生中发挥关键作用,因此通过在体内过度表达其货物受体来增强其释放,可能有助于加速伤口愈合。 」
这项研究由科大和香港理工大学(理大)的研究人员合作完成,最近于国际学术期刊《美国国家科学院院刊》 (Proceedings of the National Academy of Sciences) 上发表。 研究团队包括科大生命科学部邬振国教授、理大应用生物及化学科技学系姚钟平教授,以及他们的团队成员。

科大生命科学部副教授郭玉松(右二)和他的团队成员合照