由香港科技大学(科大)晨兴生命科学教授兼香港神经退行性疾病中心主任叶玉如教授领导的国际研究团队,发现了一种在阿尔兹海默症(AD)发病机制中起关键作用的血液蛋白,有助设计创新治疗策略,降低AD发病风险和改善AD患者病况。
目前,AD是一种不可逆转的疾病,且没有有效治疗方法,正影响全球逾5000万人口。其中一个关键障碍是,此病症的致病机制复杂且有许多未知之处,可用于开发药物的有效靶点很少。早前有研究发现,AD患者大脑中的免疫细胞(小胶质细胞),无法有效清除有害的淀粉样蛋白斑(Aβ),导致神经细胞功能失调,引起记忆丧失和认知障碍。至于排毒障碍的原因还有待深入探索。
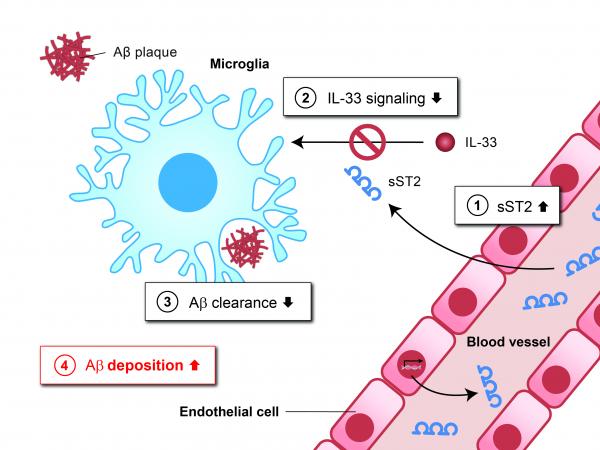
近日,叶教授领导的研究团队发现,血液中的可溶性ST2(sST2)蛋白在抑制小胶质细胞的Aβ清除起着关键作用。随着年龄增长,血液和大脑中sST2蛋白含量的增加会扰乱细胞因子白介素33(IL-33)的功效,降低小胶质细胞清除Aβ的能力,导致Aβ累积。研究团队于较早前已经发现IL-33在大脑中能够促进小胶质细胞对Aβ的清除,从而起到有益的功效。而是次团队进一步发现,降低体内sST2含量则有助防护AD,以及改善AD相关病理。
同时,研究团队还发现,sST2蛋白水平受遗传因素影响。其中,带有rs1921622基因变异的人士即使在年龄增长时,其血液和大脑中的sST2蛋白含量依旧会处于相对较低水平,因而罹患AD的风险亦较低。这种情况在带有APOE4 基因突变的女性中尤为明显(APOE4是AD的最强遗传风险因素)。根据团队所做的脑部尸检研究,带有rs1921622基因变异的人士在罹患AD时病理特征较为轻度, 即Aβ斑块沉积较少,反映其大脑中的小胶质细胞可以更有效地清除Aβ。
综合而言,这些重要发现揭示降低sST2蛋白水平可以是治疗AD的一种方法,有助研发创新治疗策略。该创新策略只须调控血液中的蛋白,与其他针对大脑的AD治疗策略相比,更简单更安全,亦为带有APOE4基因突变的女性等高危人群带来希望。据统计,带有APOE4基因突变的女性,在AD患者中占25%至50%,她们罹患AD风险更高,发病后症状更严重。
叶教授说:「是次研究进一步提高了我们对AD发病机制的理解,并为AD新药开发提供了重要靶点。由此可见,精准医学对于治疗这种多因素导致的复杂疾病至关重要。下一步工作是开发针对 sST2 的临床干预措施,评估其在预防和治疗AD方面的可行性,特别是带有APOE4基因突变、发病风险较高的女性。」
这项研究获香港特区政府的InnoHK计划支持,并由科大、伦敦大学学院和史丹福大学研究团队,以及威尔斯亲王医院、墨尔本大学和伊迪斯科文大学的临床专家合作进行。研究成果近日刊载于国际权威科学期刊《自然-衰老》,并在Alzforum等关注AD 研究的学术交流平台引发热议。
更多科大概览