(文章转载自EurekAlert!,原刊於2025年10月22日)
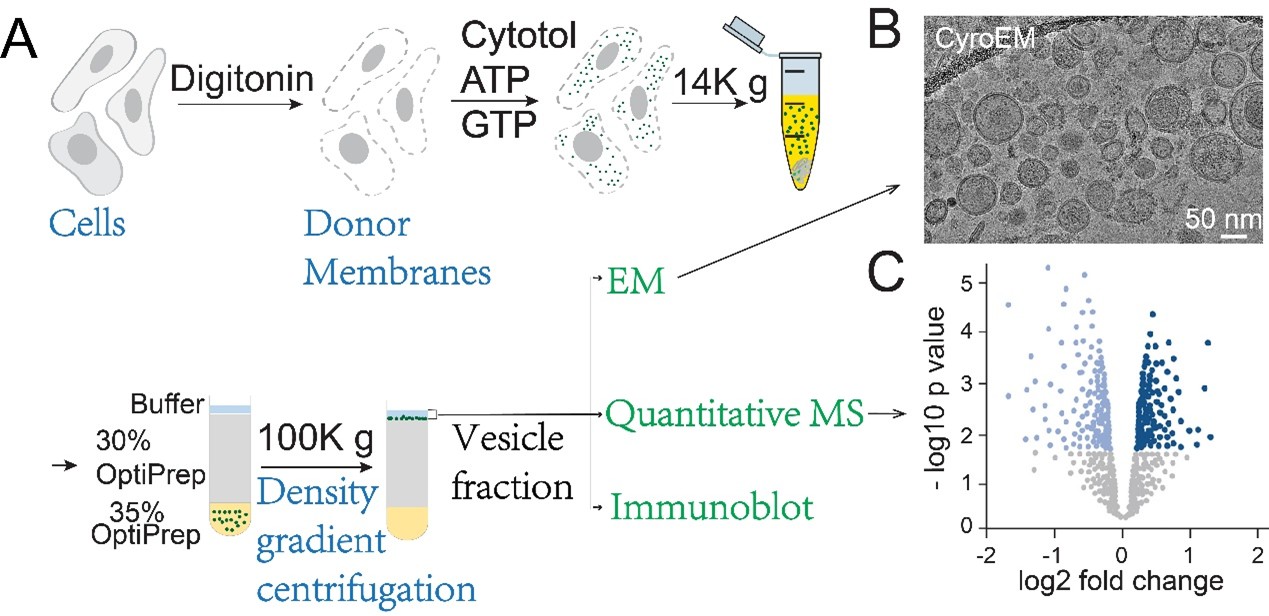
在生理学中,真核细胞的分泌途径对于维持细胞功能与生理活动至关重要,因为许多蛋白质需要通过该途径被准确运输到特定的亚细胞位置,或分泌到细胞外以发挥其功能。 香港科技大学(科大)生命科学部郭玉松教授带领的研究团队长期致力于研究分泌途径中货物蛋白被分选并装载入运输囊泡的分子机制。 该团队已成功在体外重构多种与疾病相关的货物蛋白在分泌途径中被装载入囊泡的过程,为解析货物装载的分子机制提供了重要工具。 同时,他们建立了囊泡重组体系、电子显微镜与蛋白组学的分析平台,得以有系统地鉴定囊泡的蛋白组成与形态学特征。 研究表明,该策略在发现新型货物蛋白及介导囊泡运输的细胞因子方面具有强大潜力(图一)。
郭玉松教授团队与香港理工大学(理大)姚钟平教授研究团队合作,在 《PNAS》发表了一篇研究论文,通过体外囊泡重组与定量质谱技术互相结合,有系统地鉴定了由货物适配体复合体AP-1和AP-4介导的运输货物,并解析了参与AP-4介导囊泡运输的关键细胞质调控因子。
在分泌运输路径中,高尔基体(TGN)是核心的分选枢纽,负责将蛋白质精准包装进运输囊泡。 若分选错误,货物无法抵达正确靶位,便会引发细胞极性、免疫功能及其他生理过程的缺陷。 参与高尔基体分选的关键因子之一是一类适配蛋白(AP)复合体,包括AP-1和AP-4。 这些蛋白质的基因突变与多种人类疾病密切相关:例如AP1S1(编码AP-1的 σ1 亚基)突变与MEDNIK 综合症有关; AP1S2 突变可导致 X 连锁智力障碍; 而任何AP-4亚基的突变均可引发「AP-4缺陷综合症」,这是一种复杂的遗传痉攣性截瘫。 因此,了解AP-1与AP-4的货物蛋白对于揭示其生理和病理功能具有重要意义。 然而,AP-1和AP-4所介导的货物及辅因子的完整谱系至今仍未完全阐明。 值得注意的是,AP-4 介导的高尔基输出似乎不依赖网格蛋白(clathrin),这表明囊泡形成可能还依赖尚未识别的辅助因子。
在本研究中,郭教授团队利用AP1γ1或AP4ε敲除细胞进行囊泡形成实验,分离囊泡组分,并通过定量质谱进行蛋白组学分析,由此鉴定出依赖AP-1 与AP-4的TGN 输出货物蛋白,以及AP-4介导运输所需的关键细胞质辅因子。 进一步的生化验证显示:CAB45是AP-1依赖的货物,而ATRAP(一种I型血管紧张素II受体相关蛋白)是AP-4依赖的货物; AP-4 通过识别 ATRAP 胞质末端的酪氨酸基序,介导从高尔基体装载入运输囊泡。
此外,研究发现,细胞质蛋白WDR44和PRRC1在AP-4介导的货物分选中发挥关键作用:当WDR44水平被敲低时,AP-4货物ATG9A异常聚集于高尔基体; 而敲除PRRC1则导致ATG9A滞留于内质网,损害细胞自噬功能。 同样,另一个AP-4货物(ATRAP)也在高尔基体中累积。 郭教授表示:「这些结果不仅加深了我们对AP-1和AP-4在分泌转运中功能的理解,也为系统性解析特定辅助因子的作用机制提供了强而有力的方法工具。」
该研究的共同通讯作者为科大郭玉松教授与理大姚钟平教授。 香港科技大学博士后研究员彭子晴为该研究的第一作者。